

�������գ�����ũҵ��ѧ�����������ڿ����飬�Թ㷺��������ù����ͭ�̼ٵ������е�һ����Ȼ�������ʡ������ù�ؽ����˽ṹ���Σ��ϳ���һϵ�и��Եĺ�1,3,4-�磨�f����������ù�������������Щ�������ɱ�����Խ����˲��ԣ���ؽ���ڡ�ũҩѧѧ�����Ϸ�����
�������-1-���ᣨPhenazine-1-carbonic acid��PCA����ӫ��ٵ�������Pseudomonas fluorescens����ֲ��������������������Բ�������ҹ�ע��Ϊ����ˮ���ƿݲ���ɱ����������ù�ء���PCA�����������Ⱦ�ʹٽ���̬ƽ�ⷽ�����Źؼ����á�PCA��Ϊһ������������ũҩ�����ù�����ڷ����ӻ������������������п������������Ϳ���������ԡ��俹������������2����Ļ������� ��������ڲ�ԭ��ϸ���ڱ���ԭ�Ĺ����л�����ж��ij������Ӻ������⣬�ܹ����������ĺ�ת�����ף�������ϸ�����Ե������ɻ����� ���ڷ��������ܹ���NADH��ԭ����Ϊ���Ӵ��ݵ��м��壬����ϸ����������������ԭ��
̬��NADH/NAD�����ʵȣ���Ӱ�������IJ������Ӷ�������������������������������ԡ��Ͷ��Ժ���̬�Ѻ��ԣ�PCA��ũҵ����Ҳ�õ��˹㷺��Ӧ�ã�������ɼ�����������Fusarium oxysporum��������˿�˾���Rhizoctonia solani�������ѻ�ù����Botrytis cinerea���ͺ̹���������Fusarium graminearum�������������̱���ֲ�ﵪ-�����ӻ�����ʾ������㷺��������������ԣ�һֱ��ҩ�ﻯѧ�о����ȵ㡣
1 ���ù��������ϳ�
������֮ǰ���о��У�1,3,4-�������������кܺõ�ɱ�����ԡ�����ϣ���ĺ�ѡ��������������߲�����EC50ֵΪ5.7 ��g/mL���Ƕ������յ�20%�����⣬����1,3,4-�f�������������һ���о���ʾ����500 ��g/mLʱ���Է��ѻ�ù�����ͷ���˿�˾���������ɱ�����Ժ����ԡ�������ͨ�������Ľṹ�Ż������������ӷ�ʽ����ƺϳ�����ϵ�к�1,3,4-�磨�f�������PCA��������ڻ�ø���ǰ����ɱ������������I1��I28�ĺϳ�·����ͼ1��ʾ��
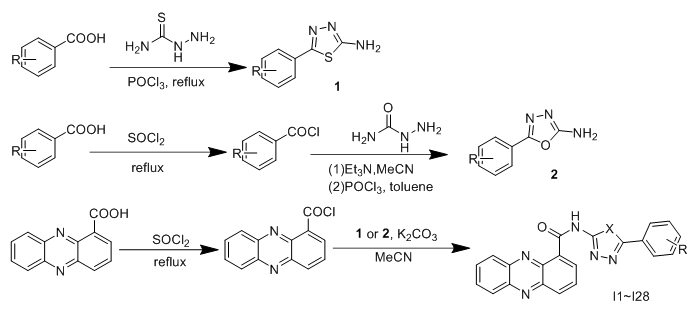
ͼ 1 ������I1��I28�ĺϳ�·��
2 ����ɱ�����Լ��
��������ƽ�巨��PDA�����������Ի�����I1��I28������ɱ�����Խ����˲ⶨ���þ�˿�������ʷ��ⶨ�����ǵ���������ʡ�PCA�������Զ�����ͬ�������½�����������˿������ȫ�ⶨ��˿ֱ���������ݹ�ʽ�����־��ʣ�I/%=(D1-D2)/D1��100��I/%Ϊ�����ʣ�D1Ϊ�հ������о�˿��ƽ��ֱ����D2Ϊ����ƽ��ֱ������PCAΪ���գ���5��ֲ�ﲡԭ����̹���������������ù������˿�˾������������ͷ��ѻ�ù���������������ɸѡ����������ⶨ�������1��������������ù��������Ժ̹���������ɱ�����Ե�EC50ֵ��33.25��99.45 ��g/mL֮�䣬�Ժ̹���������ɱ����������PCA��EC50=128.54 ��g/mL�����ر��ǻ�����I8��I11��I22�Ժ̹����������и����DZ��ɱ�����ԣ������ԼΪPCA��3��4����
�� 1 �Ե������������ѻ�ù������������ù������˿�˾��ͺ̹���������EC50ֵ����g/mL��
|
������ |
�̹������� |
������ù |
����˿�˾� |
�������� |
���ѻ�ù�� |
|
PCA |
128.54��4.68 |
7.26��1.05 |
7.56��0.99 |
12.63��1.14 |
19.76��1.31 |
|
I1 |
71.25��2.95 |
58.17��3.12 |
52.45��1.96 |
65.21��2.89 |
78.15��2.65 |
|
I2 |
78.23��3.03 |
67.15��2.24 |
64.89��2.03 |
72.15��2.35 |
89.54��3.01 |
|
I3 |
99.45��4.08 |
89.25��3.17 |
84.36��3.08 |
92.14��3.12 |
102.47��4.01 |
|
I4 |
86.12��4.11 |
72.78��2.61 |
68.58��2.64 |
78.56��3.14 |
90.13��3.12 |
|
I5 |
74.12��3.26 |
72.34��2.98 |
69.78��2.35 |
68.47��2.58 |
90.65��2.99 |
|
I6 |
98.31��3.46 |
89.17��3.22 |
97.54��3.97 |
89.22��2.64 |
120.34��3.25 |
|
I7 |
80.24��3.95 |
80.57��2.99 |
75.81��2.68 |
80.17��2.99 |
98.54��3.13 |
|
I8 |
33.25��2.06 |
31.25��2.01 |
8.64��1.11 |
25.23��1.95 |
46.28��2.01 |
|
I9 |
62.48��3.11 |
54.27��2.61 |
34.62��2.06 |
56.47��2.08 |
71.56��2.56 |
|
I10 |
49.47��2.35 |
39.46��1.94 |
15.78��1.64 |
42.13��1.97 |
61.54��2.11 |
|
I11 |
45.95��2.21 |
41.03��1.96 |
24.38��1.98 |
35.48��1.34 |
52.47��1.98 |
|
I12 |
67.36��3.12 |
55.36��1.33 |
49.31��2.08 |
65.78��2.54 |
77.67��2.31 |
|
I13 |
50.49��2.68 |
49.55��1.65 |
40.27��2.31 |
55.87��2.31 |
70.15��1.96 |
|
I14 |
84.12��3.02 |
125.34��4.74 |
82.06��3.21 |
80.49��3.21 |
128.56��4.56 |
|
I15 |
66.39��2.46 |
54.23��2.03 |
52.38��2.26 |
49.34��2.31 |
65.72��1.98 |
|
I16 |
70.23��2.34 |
57.35��1.65 |
61.26��3.06 |
50.23��2.22 |
68.23��2.35 |
|
I17 |
85.34��3.05 |
68.14��2.37 |
75.34��2.61 |
61.58��2.61 |
80.66��3.14 |
|
I18 |
76.55��2.61 |
60.89��2.16 |
63.33��2.39 |
52.36��2.13 |
74.13��3.02 |
|
I19 |
75.06��2.80 |
60.37��2.31 |
55.14��2.11 |
53.57��1.98 |
70.56��2.68 |
|
I20 |
89.61��3.22 |
71.24��3.04 |
69.46��2.49 |
63.89��3.01 |
86.49��3.28 |
|
I21 |
80.07��2.67 |
65.81��2.68 |
60.18��2.65 |
52.38��2.41 |
78.05��2.66 |
|
I22 |
46.52��3.54 |
7.24��1.01 |
26.16��2.01 |
16.56��1.34 |
45.08��2.05 |
|
I23 |
53.53��2.67 |
34.51��2.68 |
40.23��2.13 |
42.34��1.96 |
59.23��2.34 |
|
I24 |
49.97��2.39 |
22.37��1.67 |
36.72��1.94 |
31.43��1.99 |
52.11��2.16 |
|
I25 |
56.48��2.03 |
30.64��2.53 |
48.83��2.53 |
36.54��1.25 |
44.54��2.25 |
|
I26 |
53.13��2.15 |
24.35��1.84 |
30.22��1.83 |
34.13��1.67 |
51.37��1.99 |
|
I27 |
62.08��3.15 |
49.72��2.38 |
46.57��2.05 |
46.31��2.05 |
60.52��1.97 |
������Ȼ�������������ùû�����Ե��������ã���I22��EC50=7.24 ��g/mL���ԴﵽPCA��EC50=7.26 ��g/mL����ˮƽ�����⣬������I8��EC50=8.64 ��g/mL���Է���˿�˲���ɱ��������PCA��EC50=7.56 ��g/mL�����ơ��ź����ǣ�I22�Ե������ͷ��ѻ�ù����Ч��δ�ܳ���PCA�Ļ��ԣ����ڵ�����I22��EC50=16.56 ��g/mL��PCA��EC50=12.63 ��g/mL���ڷ��ѻ�ù��I22��EC50=45.08 ��g/mL��EC50=19.76 ��g/mL���Ա��ֳ��ܺõĻ��ԡ�
������ˣ�������I22�����ǹ���ɱ�����ĺ�ѡ����������I8�ǶԿ��̹��������ͷ��ѳ�ù�����ض���ѡ�����Ϊ�˽�һ��ȷ�ϱ��⻯�����������ԣ���5�����������ɱ�����Խ�����������
3 ����ɱ�����Բ���
������������ɱ�����Խ��ѡ��14������������������飬�Ե�������������˿�˾���������ù�����ѻ�ù�����ͺ̹�������5��ֲ�ﲡԭ�������������ɱ�������о���
������հ�����ȣ����������Զ���Ч��ͨ�����·���I/%=[��CK��PT��/CK]��100���㣬ʽ��IΪ��Զ���Ч����CKΪ�հײⶨ�ڼ��ƽ������ָ����PTΪ��������Ƶ�ƽ������ָ��������������2��
�����Ժ̹���������������Ծ���40.46%��58.69%֮�䣬����PCA�������ǻ�����I8��58.69%����I22��55.37%������500 ��g/mLʱ�������Ч����PCA��25.14%�����������ң��һ�����I8��91.34%���Է���˿�˾���ɱ��������PCA���ƣ�90.25%����������I22��������ù�����ѻ�ù���͵�����������ɱ�����Էֱ�Ϊ94.23%��76.38%��85.94%�����ڻ�ӽ���PCA��93.48%��90.25%��92.18%������Щ�����һ��֤ʵ�˻�����I8��I22�Ĺ���������ɱ�����ԡ�
�������������������һϵ�����ù�������ͨ�����ס�Ԫ�ط����ͺ˴Ź����Ա��⻯��������˱��������л��������������������ɱ�����Ժ�����ɱ�����ԡ��ر��ǻ�����I8��X=S��R=2-OCH3����I22��X=O��R=2-OCH3���Ժ̹���������ɱ����������PCA��������I22���й���ɱ�����ԣ���������I8��һ�������ԵĿ��̹��������ͷ��ѳ�ù���ĺ�ѡ�����
�� 2 ��������500 ��g/mLʱ��5��ֲ�����������ɱ�����ԣ�%��
|
������ |
�̹������� |
������ù |
����˿�˾� |
�������� |
���ѻ�ù�� |
|
PCA |
25.14��0.86 |
93.48��1.67 |
90.25��1.69 |
92.18��1.63 |
80.57��1.35 |
|
I1 |
45.68��1.03 |
48.21��1.07 |
60.23��1.36 |
52.14��1.02 |
35.21��0.98 |
|
I8 |
58.69��1.14 |
66.89��1.32 |
91.34��1.58 |
69.38��1.34 |
63.45��1.37 |
|
I9 |
45.69��1.03 |
50.23��1.24 |
69.16��1.35 |
52.33��1.20 |
40.12��1.25 |
|
I10 |
50.39��1.31 |
59.21��1.38 |
77.59��1.63 |
62.55��1.36 |
45.68��1.34 |
|
I11 |
52.61��1.22 |
60.33��1.39 |
68.28��1.29 |
68.16��1.64 |
56.95��1.54 |
|
I12 |
44.33��0.99 |
49.62��1.09 |
60.14��1.46 |
44.83��1.04 |
36.49��0.99 |
|
I13 |
49.61��1.21 |
55.97��1.22 |
63.21��1.43 |
45.82��1.11 |
40.55��1.06 |
|
I15 |
40.46��1.11 |
50.29��1.62 |
45.86��1.03 |
50.23��1.22 |
32.56��1.02 |
|
I22 |
55.37��1.37 |
94.23��1.98 |
76.38��1.38 |
85.94��1.86 |
48.37��1.23 |
|
I23 |
43.66��1.35 |
64.55��1.32 |
55.67��1.61 |
56.28��1.32 |
42.28��1.09 |
|
I24 |
50.15��2.01 |
70.54��1.54 |
62.13��1.30 |
60.71��1.56 |
45.68��1.37 |
|
I25 |
42.68��1.35 |
70.61��1.60 |
66.71��1.65 |
62.13��1.34 |
42.88��1.26 |
|
I26 |
35.27��0.97 |
52.68��1.34 |
51.46��1.05 |
51.04��1.05 |
38.98��0.99 |
|
I27 |
40.57��1.09 |
60.11��1.75 |
60.57��1.62 |
56.69��1.18 |
41.21��1.21 |
����Դ����ũҩѧѧ����֪������